셀트리온, 아바스틴 바이오시밀러 ‘CT-P16’ 글로벌 임상 3상 돌입
6월 국내 임상 1상 완료…포르투갈 등 20여 국가서 임상 3상 진행 계획
 윤지원⁄ 2018.08.10 11:45:47
윤지원⁄ 2018.08.10 11:45:47
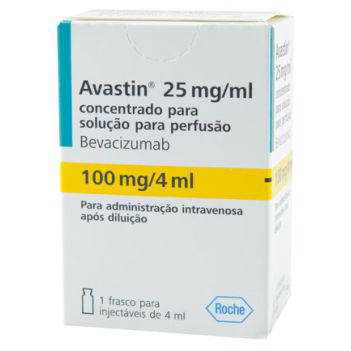
로슈의 대장암 치료제 '아바스틴'. (사진 = 로슈)
셀트리온이 대장암 치료제 ‘아바스틴(Avastin, 성분명: 베바시주맙)’ 바이오시밀러인 ‘CT-P16’의 글로벌 임상 3상에 돌입한다고 10일 밝혔다.
셀트리온은 지난 해 6월부터 1년간 국내에서 ‘CT-P16’의 안전성과 약동학 평가를 위한 임상 1상을 진행, 성공적으로 임상을 완료했으며 최근 포르투갈 의약품 허가기관(Infarmed)에 임상 3상 시험을 신청했다고 전했다.
셀트리온은 포르투갈을 시작으로 유럽, 남미 지역 등 각 국가 규제기관에 순차적으로 임상시험을 신청, 20여 개 국가 약 150 사이트에서 ‘CT-P16’의 임상 3상을 진행할 계획이다.
한편 ‘CT-P16’의 오리지널의약품인 로슈(Roche)의 아바스틴은 전이성 직결장암, 전이성 유방암, 비소세포폐암, 교모세포종 치료에 사용하는 항암제다. 로슈의 2017년 파이낸셜 리포트에 따르면 아바스틴의 지난해 세계 매출은 약 7조 5000억 원에 달한다.
셀트리온 관계자는 “셀트리온은 계획한 일정에 따라 순조롭게 아바스틴 바이오시밀러 CT-P16의 임상을 진행하고 있다”며 “CT-P16은 경쟁 바이오시밀러 대비 차별화된 경쟁력을 확보할 계획이다”라고 말했다.
- 관련태그
- CNB 씨앤비 시앤비 CNB뉴스 씨앤비뉴스
















![[특징주] 이구산업, 구리 가격 상승‧중동 리스크에 주가 강세](/data/cache/public/photos/20240416/art_159941_1713496969_170x110.jpg)