제2의 ‘발사르탄’? … ‘라니티딘’ 판매 제약사들 "걱정"
일동제약 ‘큐란’·대웅제약 ‘알비스’ 등 식약처 조사 결과 기다려
 제652호 이동근⁄ 2019.09.24 17:57:24
제652호 이동근⁄ 2019.09.24 17:57:24
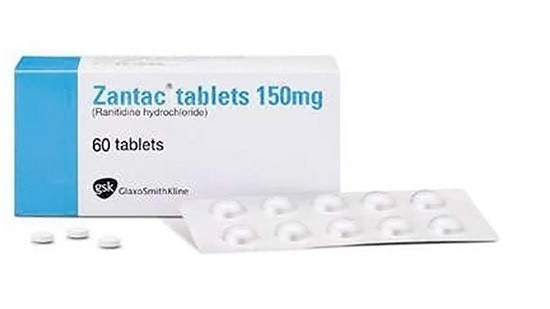
| 유명 위장약인 ‘잔탁’(성분명 : 라니티딘)에서 발암우려물질이 검출되면서 파장이 커지고 있다. 잔탁이 워낙 널리 처방되는 약이기도 하지만 과거 ‘발사르탄’제제에서 발암물질이 검출된 뒤 국내 제약업계가 적지 않은 피해를 입은 바 있어 유사한 사태가 벌어지는 것 아니냐는 우려가 업계에서 나오는 것이다. 현재 업계에서는 식품의약품안전처의 빠른 조사 결과를 기다리는 한편, 추후에도 이같은 사태가 벌어지는 것 아니냐는 걱정도 나온다. ‘라니티딘’ 사태를 바라보는 업계의 모습을 cnb저널에서 들여다 보았다. |

소위 ‘라니티딘’ 사태는 지난 9월 13일(미국 현지 기준) 미국FDA와 유럽의약품청(EMA)이 글락소스미스클라인(GSK)의 잔탁에서 ‘N-니트로소디메틸아민’(NDMA)이 검출됐다고 발표하면서 시작됐다. NDMA는 WHO 국제 암연구소(IARC) 2A 물질(인간에게 발암물질로 작용할 가능성 있는 물질)이다.
이후 한국 식약처는 미국 FDA가 미량 검출되었다고 발표한 라니티딘 제품중, 우선 한국 GSK가 허가 받은 잔탁 3개품목(일반의약품 75㎎·전문의약품 150㎎·주사제2㎖)과 잔탁에 사용된 원료 라니티딘(6개)을 긴급하게 수거·검사를 실시한 결과 NDMA가 검출되지 않았다고 16일 밝혔다.
그러나 식약처가 현재 수입 또는 국내 제조되는 모든 라니티딘 원료(원료 제조소 11개소)와 해당 원료를 사용한 의약품(395품목)을 대상으로 계속해서 수거·검사를 확대 실시할 계획이라고 밝히면서 국내 제약사들을 우려에 빠뜨렸다.
NDMA는 지난해 고혈압치료제 원료인 ‘발사르탄’ 중 중국 수입산에서 발견돼 논란을 일으켰던 물질이다. 당시 국내 발사르탄 제제 중 총 175개 품목이 판매금지 처분을 받았다.
오래전부터 처방돼 시장 영향 커 … 복합제도 피하지 못해
라니티딘 논란이 심각하게 받아들여지는 이유는 발사르탄 못지않게 널리 처방되던 약이기 때문이다. 라니티딘은 위산과다, 속쓰림, 위·십이지장궤양, 역류성식도염 등에 사용하는 의약품으로 오래전부터 사용돼 온데다, 다른 약물 복용 시 속쓰림 등을 예방하기 위해서도 많이 처방된다.
국내에서 시판 중인 라니티딘 단일제는 국산 162품목(99개소), 수입 3품목(2개소)에 달하며 복합제는 230폼목(139개소)에 달한다. 식약처에 따르면 지난해 수입 및 생산실적 기준으로 위장병(소화성궤양) 치료제는 약 1조 511억원이며, 이 중 라니티딘 함유 의약품은 2664억 원으로 25.3%에 달한다.
현재 국내 제품 중에서는 단일제 기준 일동제약 ‘큐란’이 시장 점유율 1위이며, 복합제 중에서는 대웅제약 ‘알비스’(라니티딘·비스무트시트르·수크랄페이트)가 점유율 1위를 기록하고 있다. 이들 제품의 지난해 매출은 큐란이 약 200억 원, 알비스가 약 380억 원에 달한다.
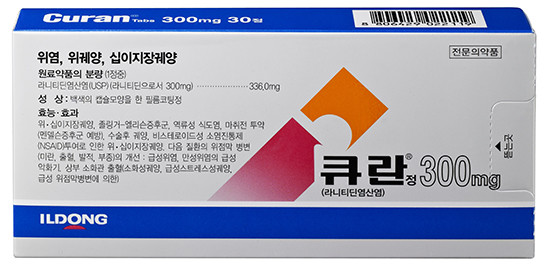
국내 제약업계 관계자는 “라니티딘 제제가 워낙 오래된 약이다 보니 매출액에서 보이는 것보다 처방량이 많다”며 “특정 제약사는 라니티딘 관련 매출이 전체 매출의 약 4분의 3 정도에 달한다는 이야기도 들었다”고 설명했다.
일단 업계는 식약처의 검사 결과를 기다려 본다는 분위기다. 사전에 어떤 대응을 한다는 것이 부담스럽다는 것이다. 다만 대웅제약의 경우 약사들에게 ‘알비스’의 라니티딘에 대한 검사 결과를 공표하며 적극적으로 대응하고 있다.

대웅제약이 의료계에 보낸 공문에 따르면 알비스에 들어가는 라니티딘을 생산하는 인도 Orchev사는 자체적으로 검사한 결과 NDMA가 불검출 수준에 가까운 0.0069ppm으로 나타났다. 이는 라니티딘 300㎎ 복용시 NDMA의 허용기준인 0.32ppm 대비 충분히 낮으며 인체에 유해하지 않은 수준이라고 대웅제약 측은 설명했다.
또 대웅제약은 식약처와 별개로 외부 분석기관에 검사를 의뢰 했으며, 조만간 결과를 발표한다는 입장이다.
검사 결과 나오기 전부터 ‘대체처방’ 언급
제 3, 제 4의 ‘발사르탄 사태’ 우려도
문제는 식약처의 검사 기간이 길어질 경우 아예 라니티딘 제제의 처방을 기피하는 분위기까지 형성될 수 있다는 것이다. 실제로 대한의사협회는 24일 “의사와 의료기관은 환자의 라니티딘 계열 의약품 교체 요구 시 우선적으로 다른 약물을 처방해 달라”고 공지했다.
대체약물이 적지 않다는 점도 라니티딘 관련 제약사들의 우려를 키우고 있다. 대표적인 약물이 양성자펌프억제제(Proton pump inhibitors, PPI)제제로 국산약 중에는 한미약품 ‘에소메졸;’, 일양약품 ‘놀텍’ 등이 있다. 최근 출시된 CJ헬스케어의 신약 ‘케이캡’(테고프라잔) 등 P-CAB 제제도 처방이 가능한 것으로 알려져 있다.
업계에서는 앞으로 이와 비슷한 문제가 계속 발생할 수 있다는 전망이 나온다. 기술 발전에 따라 검사법이 갈수록 정교해 지면서 과거에는 큰 문제가 없었던 약물들도 문제가 발견되고 있어 앞으로 제 3, 제 4 의 발사르탄 사태가 나타나지 않으리라는 법이 없어서다.
제약업계 관계자는 “라니티딘을 비롯해 상당수의 원료의약품에서 NDMA가 검출되는 것은 제조 과정에서 영향을 받은 것으로, 갈수록 비슷한 사례가 나타나지 않으리라는 법이 없다”며 우려를 표한 뒤“사실 NDMA가 위해기준 이하로 발견된 경우에도 판매정지 등의 조치가 이뤄지고 있어 회사 측에서는 억울한 면도 있겠지만 소비자들의 수준이 높아졌기 때문에 식약처도 어쩔 수 없을 것”이라고 덧붙였다.
- 관련태그
- CNB 씨앤비 시앤비 CNB뉴스 씨앤비뉴스














![[특징주] HD현대중공업, 한화오션, 삼성중공업 조선주 급등](/data/cache/public/photos/20241145/art_164653_1731022611_170x110.jpg)
![[특징주] 토모큐브 상장 첫날 37.06% 급락...어제 더본코리아와 대비](/data/cache/public/photos/20241145/art_164651_1730962773_170x110.jpg)


![[특징주] 역시 백종원! 더본코리아, 신규 상장주 하락 신화 깼다!](/data/cache/public/photos/20241145/art_164618_1730875336_170x110.jpg)






















